CRISPR/Cas9基因編輯提高超聲癌癥治療的有效性
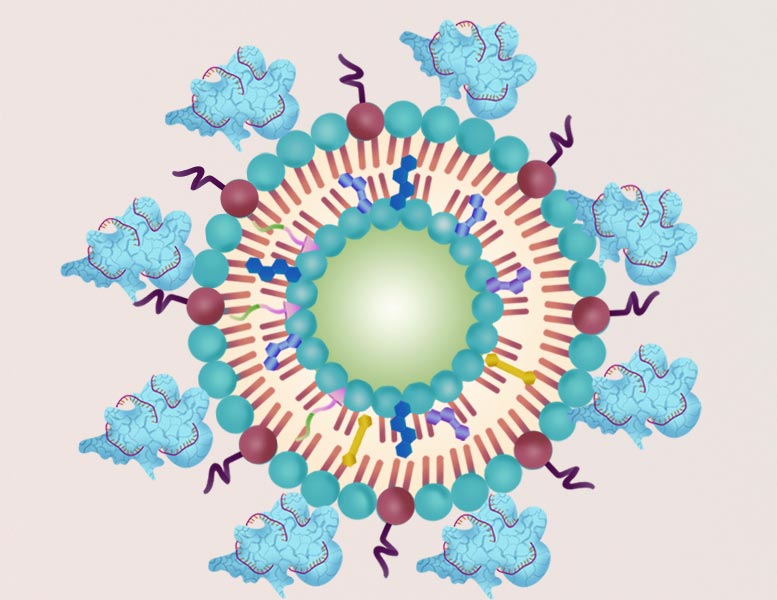
對腫瘤進行超聲波照射會導致脂質納米顆粒(如上圖所示)釋放有害的 ROS 和 CRISPR/Cas9 基因編輯系統。學分:改編自 ACS Central Science 2021,D??OI:10.1021/acscentsci.1c01143
聲動力療法使用超聲波與藥物結合在腫瘤部位釋放有害的活性氧 (ROS)。然而,這種治療并不是很有效,因為癌細胞可以激活抗氧化防御系統來抵消它。現在,在ACS Central Science上報道的研究人員已經通過 CRISPR/Cas9 基因編輯突破了這些防御,使聲動力療法能夠有效地縮小肝癌小鼠模型中的腫瘤。
肝細胞癌是最常見的肝癌形式,預后較差,通過切除部分肝臟或移植健康肝臟的手術治療不適合疾病更晚期的患者。由于超聲波可以深入組織內部,因此聲動力療法可能是治療肝細胞癌的一種有效的非侵入性方法。但目前,癌細胞可以通過激活一種叫做核因子紅細胞2相關因子2(NFE2L2 )的基因來迅速克服這種療法。),它部署了細胞的解毒和抗氧化酶防御。CRISPR/Cas9 基因編輯技術已被用于在實驗室中敲除基因表達。因此,Wei Feng、許慧雄、Yu Chen 及其同事想知道他們是否可以通過使用這種技術降低NFE2L2表達來提高聲動力療法的有效性。
作為第一步,研究人員將 CRISPR/Cas9 系統和 ROS 前體分子封裝在脂質納米顆粒中。然后,他們用納米顆粒處理培養皿中的肝細胞癌細胞。脂質納米顆粒被細胞的溶酶體吸收。超聲處理導致 ROS 形成,使溶酶體破裂,使 CRISPR/Cas9 系統進入細胞核并抑制NFE2L2基因表達。活性氧還破壞了其他細胞成分。結果,與沒有NFE2L2基因編輯的情況相比,聲動力療法導致更多的癌細胞死亡。
接下來,該團隊將納米粒子治療注射到植入了人類肝細胞癌腫瘤的小鼠體內。在納米粒子和超聲波聯合治療 15 天后,小鼠體內的所有腫瘤都消失了,并且沒有復發。單獨接受聲動力學治療的小鼠比未治療的小鼠腫瘤更少,但添加 CRISPR/Cas9 系統顯著提高了治療的有效性。研究人員說,由于基因編輯只發生在超聲波照射下的腫瘤組織中,因此不會導致健康組織中的基因突變。
參考:
“超聲控制的 CRISPR/Cas9 系統增強肝細胞癌的聲動力治療”,作者 Haohao Yin、Liping Sun、Yinying Pu、Jifeng Yu、Wei Feng、Caihong Dong、Bangguo Zhou、Dou Du、Yan Zhang、Yu Chen 和 Huixiong Xu , 2021 年 12 月 8 日,ACS 中心科學。
DOI: 10.1021/acscentsci.1c01143
作者感謝中國國家自然科學基金委員會和上海市衛生健康委員會的資助。